סטודנטים מתוכנית המצטיינים של הפקולטה להנדסה, בהנחיית ד"ר ביסקר, פיתחו סימולציית מחשב לחיזוי הדינמיקה של מערכות ביולוגיות מחוץ לשיווי משקל תרמודינמי

בחר הכל
משפטים
כללי
הנדסה
חיי הקמפוס
ASV
מערכות קוונטיות
תחבורה חכמה
רכב אוטונומי
קול קורא
מכונת הנשמה
COVID-19
מטא-חומרים...
הנדסת חשמל
הנדסה מכנית
אולטרה-סגול
אולטרה-סגול
RoboBoat
MRI
בחר הכל
פרס
ברכות
כנס
מחקר
מחקר בפקולטה
פוקוס

מחקר
סטודנטים מתוכנית המצטיינים של הפקולטה להנדסה, בהנחיית ד"ר ביסקר, פיתחו סימולציית מחשב לחיזוי הדינמיקה של מערכות ביולוגיות מחוץ לשיווי משקל תרמודינמי

עדי בן-ארי ולירון בן-ארי הם סטודנטים להנדסת חשמל ופיזיקה, בשנה ד' ובתוכנית המצטיינים של הפקולטה להנדסה. אין זה במקרה שיש להם שם משפחה זהה, מדובר על תאומים זהים עם גאווה כפולה במיוחד לאור העובדה שמאמרם פורסם לראשונה החודש במגזין המדעי והיוקרתי The Journal of Chemical Physics. המאמר נכתב בהנחייתה של ד"ר גילי ביסקר, בנושא: "Nonequilibrium self-assembly of multiple stored targets in a dimer-based system"
ד"ר ביסקר מפתחת במעבדה שלה ננו-חיישנים אופטיים תוך שימוש בתכונות האופטיות של ננו-צינוריות מפחמן כדי לזהות ולכמת מולקולות ביולוגיות בצורה ספציפית וסלקטיבית. בנוסף, היא חוקרת מערכות מורכבות מחוץ לשיווי משקל תרמודינמי, בהשראת מערכות ביולוגיות.
מערכות הרכבה עצמית
במערכות רבות, ובפרט בגוף האדם, מתרחשים תהליכים של הרכבה עצמית – תהליכים בהם מספר אבני בניין, כמו חלבונים, מסתדרים במבנה מסוים שנחוץ לפעולה ביולוגית ספציפית. כאשר תהליכי הרכבה עצמית מתרחשים בשיווי משקל תרמודינמי, כאשר חום נכנס מהסביבה או יוצא אליה רק באופן איטי ומבוקר, ניתן לתאר אותם ולחזות את תוצאותיהם מתוך התורה של מכניקה סטטיסטית בשיווי משקל.
אולם, תהליכים בגוף האדם מתאפיינים בחוסר שיווי משקל ואינם הפיכים, מה שמצריך כלים מתקדמים יותר על מנת לנתח אותם. במחקר, מודלה מערכת כללית של אבני בניין משני סוגים שונים שיכולות לשחזר מספר מבני מטרה, בהשראת מערכות ביולוגיות.
באמצעות סימולציות מחשב של המערכת, בהן הדינמיקה הוצאה משיווי משקל על ידי כוח לוקאלי (מקומי) – שמשפיע על האינטראקציה בין אבני בניין שכנות, הצליחו החוקרים להדגים מספר תכונות מעניינות. למשל, התאפשרה הרכבה של מבני המטרה מתוך מבנים התחלתיים קטנים יותר ביחס לאלו הנחוצים בשיווי משקל, הוגדלו מספר מבני המטרה שניתן לקודד למערכת, וכן שופרו היציבות ומהירות ההרכבה.
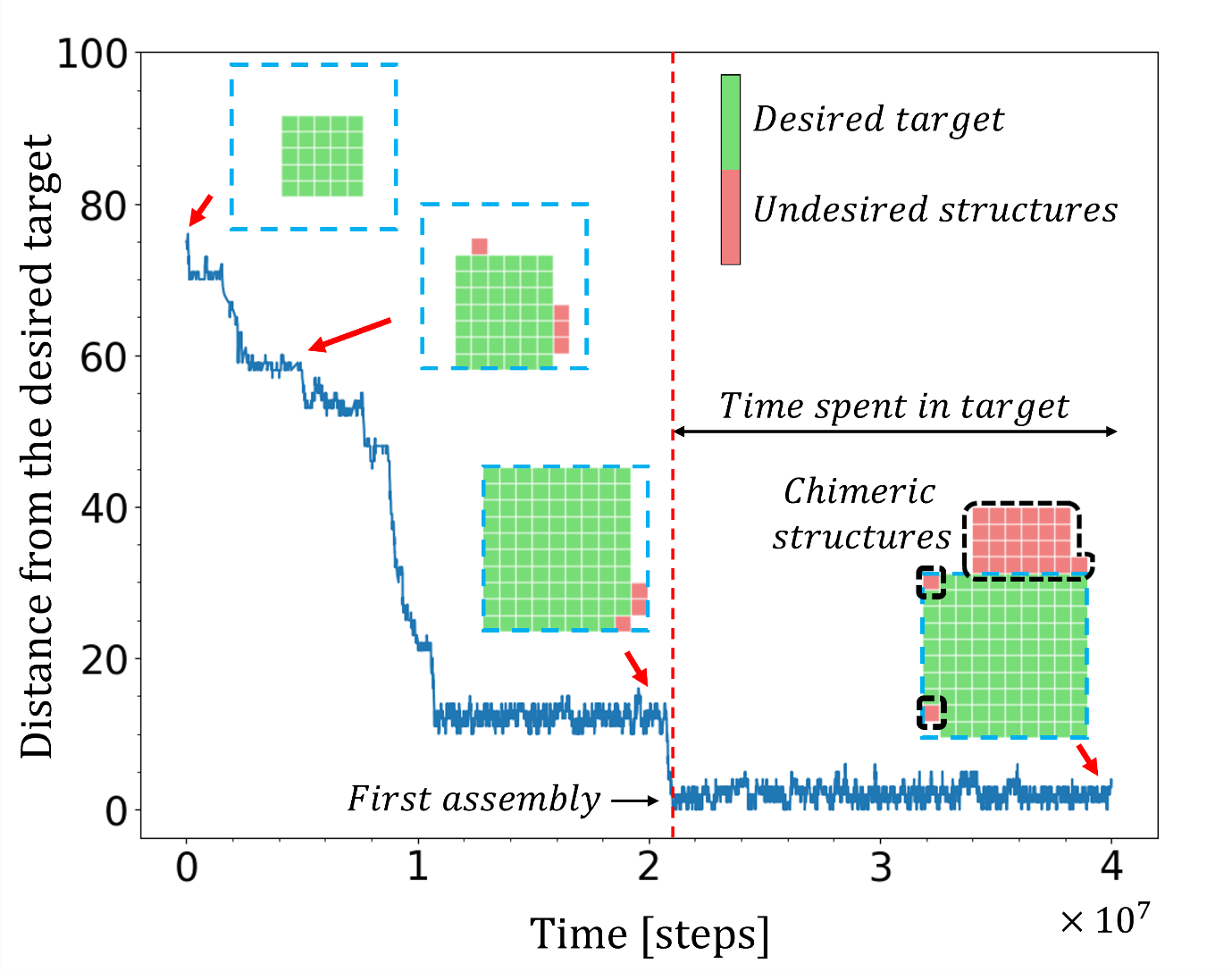
איור מתוך המאמר: סימולציה של הדינמיקה של המערכת. ככל שהזמן עובר, מצטרפים עוד חלקיקים לגרעין ההתחלתי ומבנה המטרה מורכב. בנוסף לחלק שחופף למבנה המטרה (בירוק), נבנים גם מבנים שגויים, שאינם שייכים למבנה המטרה (באדום).
איך המחקר יכול לסייע בעתיד?
מחקר זה יוכל לסייע בתכנון ושיפור מערכות המסוגלות לאחסן מספר מבני מטרה ולשחזר אותם, למשל חומרים מסתגלים שיכולים להסתדר במבנים שונים כתלות בתנאים חיצוניים. בפרט, הקטנת המבנים ההתחלתיים הדרושים, כפי שהוצג במחקר, יכולה להוות בסיס לאחסון יעיל יותר של מידע באמצעות מערכות מורכבות.
אלה שמתאהבים בבעיה הם אלה שממציאים לה פתרון

מחקר
לראשונה, חוקרות מהנדסה ביו-רפואית הצליחו בעזרת ננו-צינוריות מפחמן לבצע מעקב בתוך תולעים מבלי שתהיה הפרעה של אוטופלורנסציה מהתולעת עצמה

מולקולות או חלקיקים פלורסנטים, הפולטים אור באורך גל מסויים בעקבות עירורם באור בעל אורך גל קצר יותר, מהווים כלי נפוץ במחקרים רבים. לרוב, חוקרים משתמשים בצבענים פלורסנטים על מנת לסמן ולעקוב אחר חלבונים או מטרות ברקמות שונות בתוך חיות מודל. במקרה של תולעים, הסימון לא פשוט בכלל, היות ולתולעת עצמה יש חלבונים שפולטים פלורסנציה בתחום האור הנראה באורכי גל זהים לאורכי הגל בהם פולטים הצבענים הפלורסנטיים.
בעזרת פיתוח חדש, המבוסס על ננו צינוריות מפחמן של ד"ר ביסקר, הודגמה יכולת דימות ומעקב בתוך התולעים מבלי שתהיה הפרעה של אוטופלורנסציה מהתולעת עצמה, בזכות הפליטה הפלורסנטית של ננו-הצינוריות בתחום האינפרא-אדום הקרוב.
עבודתה של ד"ר גילי ביסקר ומנהלת המעבדה שלה ד״ר עדי הנדלר-נוימרק בנושא, התפרסמה בכתב העת המדעי Materials Today Bio בה הן חושפת את השיטה החדשנית למעקב אחר ננו-הצינוריות מפחמן בתוך תולעים. במחקר הייתה שותפה גם ד״ר ורנה וולף, פוסטדוקטורנטית במעבדתה של גילי.
ד"ר ביסקר מפתחת במעבדה שלה ננו-חיישנים אופטיים תוך שימוש בתכונות האופטיות של ננו-הצינוריות מפחמן כדי לזהות ולכמת מולקולות מטרה בצורה ספציפית וסלקטיבית. החיישנים מבוססים על ננו-צינוריות מפחמן הפולטות פלורסנציה בתחום האינפרא-אדום הקרוב, וכך מתאפשר לראות עמוק יותר בתוך הרקמה ובדוגמאות ביולוגיות, ולשפר את היחס בין האות לרעש.
תולעים כחיית מודל
תולעים משמשות חיית מודל נפוצה בזכות דמיון גנטי גבוה לבני אדם בגנים מחוללי מחלות כמו למשל במחלת הפרקינסון. למרות היתרונות הרבים שלהן כגון גודלן הקטן ושקיפותן, חסרון אחד משמעותי הוא האוטופלורסנציה שלהן בכל התחום הנראה, הנובעת מחלבונים שנמצאים בתוך התולעת עצמה הפולטים פלורסנציה. חסרון זה קיים לא רק בתולעים, אלא בחיות מודל רבות, עובדה המקשה מאוד על שימוש בצבענים או חלבונים פלורסנטים סינתטיים, היות ולא ניתן להפריד בין החלבונים הפלורסנטים הטבעיים של האורגניזמים לבין הצבען הפלורסנטי הסינתטי.
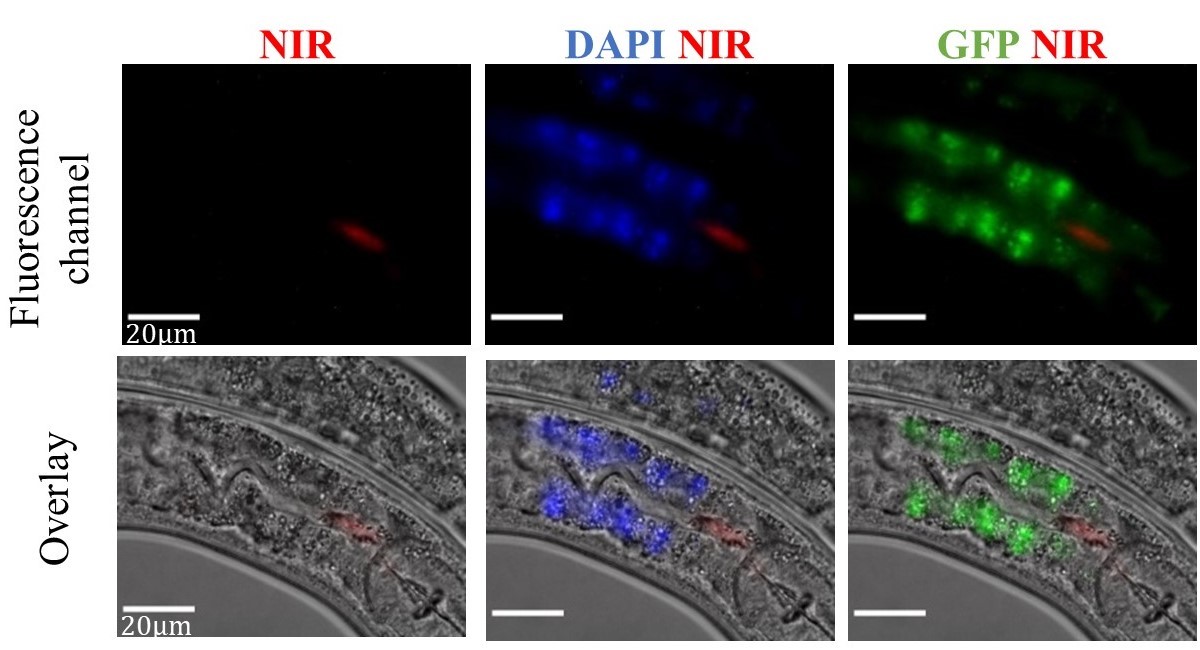
תמונה מהמאמר: בשורה העליונה ניתן לראות תמונות פלורסנטיות של התולעים במספר אורכי גל, התמונה השמאלית (NIR) היא של ננו-הצינוריות (אדום). התמונה האמצעית (DAPI+NIR) והימנית (GFP+NIR) הן תמונות משולבות של ננו-הצינוריות מפחמן באדום עם התמונות של האוטופלורסנציה של התולעת באורך גל המתאים לצבע הפלורסנטי הסינתטי DAPI או GFP (כחול או ירוק). בשורה השנייה התמונות הפלורסנטיות מוצגות על גבי תמונה באור לבן של התולעים, על מנת למקם את ננו-הצינוריות ביחס למעי של התולעת.
החוקרות השתמשו בננו-צינוריות מפחמן אשר פולטות פלורסנציה בתחום האינפרא אדום הקרוב – זהו תחום ספקטרלי בו אין אוטופלורסנציה כלל. "באמצעות ננו-הצינוריות הצלחנו לעקוב אחר פעילות העיכול של התולעים, לראות את המעבר שלהן בוושט עד צינור המעי, ולנטר את פעילות השאיבה של האוכל", מסבירה ד"ר הנדלר-נוימרק.
לדברי ד״ר ביסקר, ״הננו-חלקיקים הללו מתאימים לעבודה עם דוגמאות ביולוגיות ואינם פוגעים בהן, ולכן מאפשרים לעקוב אחר תהליכים בתוך אורגניזמים או תאים חיים ללא הפרעה של האוטופלורנסנציה הטבעית שלהם. השימוש בננו-צינוריות מפחמן יכול להוות יתרון משמעותי במעקב אחר תהליכים בחיות מודל קטנות כמו תולעים וגם לעקוף לחלוטין את האתגר של אוטופלורסנציה בתחום האור הנראה״.
אלה שמתאהבות בבעיה הן אלה שממציאות לה פתרון
מחקר
המחקר נערך בשיתוף חוקרים מהנדסה ביו-רפואית, בית הספר סגול למדעי המוח, מדעי המחשב והאוניברסיטה העברית

כמעט שנתיים אחרי שהפכה למגפה עולמית, שקטלה מיליוני בני אדם, עדיין לא נפתרה התעלומה אילו חלבונים בנגיף ה-SARA-CoV-19 אחראים לנזק החמור לכלי הדם שעשוי אף להוביל להתקף לב או לשבץ. כעת, צוות מומחים בהובלת אוניברסיטת תל אביב הצליח לזהות לראשונה חמישה חלבונים מבין 29 החלבונים המרכיבים את הנגיף שאחראים לפגיעה בכלי הדם. החוקרים מקווים כי זיהוי החלבונים יסייע בפיתוח תרופות ייעודיות לקורונה ויביא להפחתת הפגיעה בכלי הדם.
המחקר נערך בהובלת קבוצות המחקר של ד"ר בן מעוז מהמחלקה להנדסה ביו-רפואית ובית הספר סגול למדעי המוח, פרופ' אורי אשרי מבית הספר סגול למדעי המוח והפקולטה למדעי החיים, ופרופ' רודד שרן מבית הספר למדעי המחשב ע"ש בלווטניק - כולם חוקרים באוניברסיטת תל אביב. במחקר השתתפו גם פרופ' יעקב נחמיאס מהמכון למדעי החיים באוניברסיטה העברית, והחוקרים ד״ר רוסאנה ראוטי, ד״ר יעל ברדוגו והדוקטורנט מיישר שחוח מאוניברסיטת תל אביב. תוצאות המחקר החדש התפרסמו בכתב העת eLife.
"אנחנו רואים שכיחות גבוהה מאוד של מחלות כלי דם וקרישת דם, דוגמת שבץ והתקף לב, בקרב חולי קורונה", מסביר ד"ר בן מעוז. "אנחנו רגילים לחשוב על קורונה כעל מחלה נשימתית בעיקרה, אבל האמת היא שחולי קורונה נמצאים בסיכון מוגבר עד פי שלושה לעבור שבץ או התקף לב למשל. כל העדויות מראות שהנגיף פוגע קשות בכלי הדם או בתאי האנדותל העוטפים את כלי הדם. אלא שעד היום התייחסו לנגיף כולו כאל מקשה אחת. אנחנו רצינו לגלות אילו חלבונים בתוך הנגיף אחראים לנזק הזה".
נגיף הקורונה החדש הוא נגיף פשוט יחסית – והוא מורכב בסך הכול מ-29 חלבונים שונים (לעומת עשרות אלפי חלבונים שמייצר גוף האדם). החוקרים מאוניברסיטת תל אביב השתמשו ב-RNA של כל אחד מחלבוני הקורונה ובדקו את התגובה שנוצרת כאשר מחדירים את רצפי ה-RNA השונים לתאים אנושיים של כלי דם במעבדה, וכך הצליחו לזהות חמישה חלבוני קורונה שפוגעים בכלי הדם.
"כשנגיף הקורונה חודר לגוף, הוא מתחיל לייצר 29 חלבונים, נוצר נגיף חדש, הוא מייצר 29 חלבונים חדשים וכך הלאה", מספר ד"ר מעוז. "בתהליך הזה, כלי הדם שלנו הופכים מצינורות אטומים למעין רשתות או חתיכות בד חדירות, ובמקביל חלה הגברה בקרישת הדם. אנחנו בדקנו ביסודיות את ההשפעה של כל אחד מ-29 החלבונים שהנגיף מבטא, והצלחנו לראשונה לזהות חמישה חלבונים ספציפיים שמחוללים את הנזק הגדול ביותר לתאי האנדותל ומכאן גם ליציבות ולתפקוד כלי הדם. בנוסף, השתמשנו במודל חישובי שפותח על ידי פרופ' שרן, המאפשר לשער ולזהות אילו מחלבוני הקורונה הם בעלי ההשפעה הגדולה ביותר על רקמות נוספות פרק לכלי הדם, וזאת מבלי שראינו אותם ב'פעולה' במעבדה".
לדברי ד"ר מעוז, לזיהוי החלבונים עשויות להיות השלכות משמעותיות במאבק במחלה. "המחקר שלנו יכול לסייע במציאת מטרות לתרופה שתשמש לעצירת פעילותו של הנגיף, או לפחות למזעור הנזק בכלי הדם".

מחקר
החוקרים, בהובלת פרופ' תמיר טולר וסטודנטית המחקר טל גוטמן הצליחו לנבא את סוג הסרטן ואת שיעור התמותה ממנו לפי מוטציות "שקטות" בגנומים הסרטניים – הוכחת היתכנות שיכולה בעתיד להציל חיי

מוטציות "שקטות" מוגדרות ככאלה שלא משנות את רצף חומצות האמינו של החלבונים. בשנים האחרונות מצטברות הראיות לכך שמוטציות שקטות, הן בתוך והן מחוץ לאזור הקידוד הגנטי בתא, יכולות להשפיע על ביטוי גנים וכי ייתכן שהן קשורות להתפתחות ולהתפשטות של תאים סרטניים. עם זאת, עד כה לא נבדק כמותית האם המוטציות הללו יכולות לתרום לזיהוי סוג הסרטן ולניבוי סיכויי השרידות של החולה.
במחקר החדש, המבוסס על כשלושה מיליון מוטציות מגנומים סרטניים של 9,915 חולים, החוקרים ניסוי לבדוק האם הם יכולים לזהות את סוג הסרטן ולהעריך את שיעור התמותה ממנו 10 שנים לאחר האבחנה הראשונית אך ורק על סמך המוטציות השקטות – ומצאו כי יכולת הפרדיקציה של המוטציות השקטות דומה בהרבה מיקרים לביצועי הפרדיקציה המקובלת של המוטציות ה"רגילות". בנוסף ניסו החוקרים להעריך האם שילוב של מידע על מוטציות שקטות ורגילות יכולות לשפר יכולת הסיווג של סוג הסרטן, ומצאו כי המידע שמתקבל ממוטציות שקטות משפר את מרווח הטעות ב-68%. בסוגים מסוימים של סרטן מדובר בשיפור של עד 17% ביכולת הסיווג, כאשר שילוב שני סוגי המוטציה יכול לשפר את הפרוגנוזה בשיעור של עד 5%.
"בגנום שלנו, כמו בכל גנום של כל יצור חי אחר, ישנן מוטציות שיכולות לשנות את רצף חומצות האמינו של החלבונים שמקודדים בגנום", מסביר פרופ' טולר. "מאחר שהחלבונים הללו אחראים על המנגנונים השונים בתא, מוטציות כאלה מעורבות בהפיכת התא הבריא לתא סרטני. לעומתן, יש מוטציות שלא משנות את חומצות האמינו, ולכן קראו להן 'שקטות' והתעלמו מהן במשך שנים רבות. אנחנו ערכנו בפעם הראשונה אנליזות לכ-10,000 גנומים סרטניים מכל הסוגים, והראינו שיש למוטציות השקטות ערך דיאגנוסטי, איזה סוג סרטן זה, וגם ערך פרוגנוסטי, כמה זמן החולה ישרוד".
לדברי פרופ' טולר, החומר הגנטי בתא מחזיק בשני סוגים של מידע: מה רצף חומצות האמינו שמיוצר – ומתי וכמה לייצר מכל חלבון – כלומר הרגולציה של תהליך הייצור. "אותן מוטציות שקטות יכולות להשפיע על הרגולציה של ביטוי גנים, וזאת השפעה לא פחות חשובה מסוג החלבון שמיוצר. מן הסתם אם התא מייצר הרבה פחות מחלבון מסוים – זה גרוע כמעט כמו למחוק אותו. השפעה נוספת היא קיפול החלבון. החלבון הוא מולקולה ארוכה שכוללת בדרך כלל מאות רבות של חומצות אמינו, כאשר הקיפול התלת ממדי של המולקולה מתחיל כבר כשהן מיוצרות בריבוזום. קצב הייצור של החלבון על ידי הריבוזום משפיע על הקיפול, והמוטציות השקטות יכולות להשפיע על קצב הייצור של החלבון ולכן על הקיפול שלו – קיפול שהוא משמעותי לתפקוד בפועל. בנוסף, יש מקרים בהם המוטציות השקטות משפיעות על תהליך בשם שיחבור, שבו חתיכות מהחומר הגנטי נחתכות ליצירת הרצף הסופי שממנו ייווצר החלבון. בקיצור, מסתבר שהמוטציות השקטות האלה עושות הרבה מאוד רעש, ואנחנו הצלחנו לראשונה לכמת את ההשפעה שלהן".
כדי לבחון את השערתם ולכמת את השפעת המוטציות הללו, פרופ' טולר ועמיתיו השתמשו במידע גנטי ציבורי על גנומים סרטניים מהמכונים הלאומיים לבריאות (NIH) בארה"ב. החוקרים לקחו הנתונים על הגנום הסרטני וניסו בשיטות המבוססות על למידת מכונה לנבא מה סוג הסרטן וכמה שנים חי כל חולה לפי המוטציות השקטות – ולאחר מכן השוו את התוצאות שקיבלו לנתוני האמת מהמאגר.
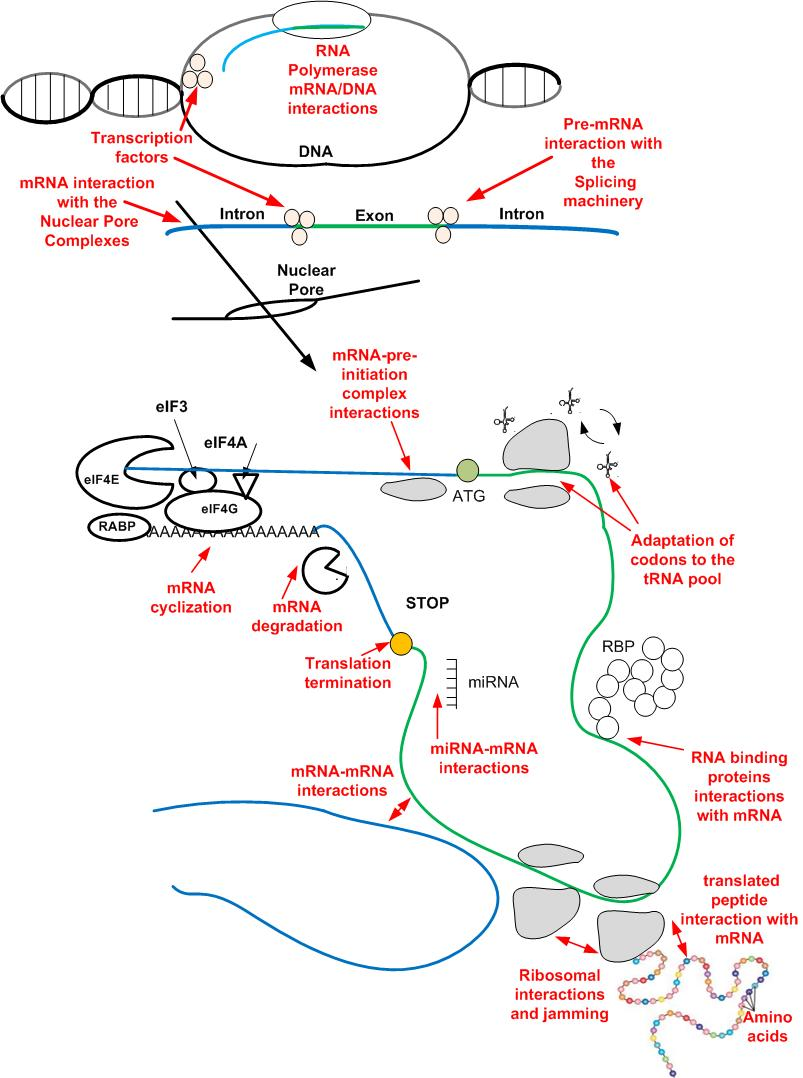
תמונה: אילוסטרציה של אינטראקציות שונות של החומר הגנטי עם פקטורים בתא שמבקרים את רמות הביטוי. מוטציות שקטות יכולות להשפיע על יעילות האינטראקציה עם הפקטורים האלה בתא הסרטני, ולכן להשפיע על רמות הביטוי של גנים שמשפיעים על השרידות של התא הסרטני.
"לתוצאות המחקר מספר השלכות חשובות", אומר פרופ' טולר. "קודם כל שימוש במוטציות שקטות בהחלט יכול לשפר מודלים שחוזים פרוגנוזה ומשמשים לסיווג. חשוב לציין שגם לשיפור של 17% יש משמעות גדולה מאוד כי מאחורי המספרים האלה עומדים בני אדם שאנחנו אוהבים, ויום אחד אולי אנחנו עצמנו, לכן כל שיפור של אחוז הוא דרמטי. רופא שמגלה גרורות רוצה לדעת מה מקור הגרורה ומה מסלול התפתחות המחלה, כדי להתאים את הטיפול הטוב ביותר. אם למשל במקום דיאגנוסטיקה ופרוגנוסטיקה שגויות לחמישה מבין עשרה חולי סרטן נגיע למצב שבו שוגים רק בארבעה מכל עשרה חולי סרטן, זה יכול להיתרגם בסופו של דבר למיליוני חולים שאולי ניתן להציל את חייהם. בנוסף, התוצאות שלנו מראות שרק על סמך מוטציות שקטות ניתן במקרים רבים לקבל ביצועי ניבוי דומים להסתמכות על מוטציות שהן לא שקטות. זו תוצאות מעודדת, מכיוון שבשנים האחרונות מפותחות טכנולוגיות שמסווגות סרטן על סמך בדיקות דם לא פולשניות יחסית, המבוססות על אנליזה של חתיכות דנ"א ממקור סרטני. מאחר שרוב הדנ"א שלנו לא מקודד לחלבון, סביר להניח שרוב החתיכות מסוג זה שנדוג יכילו מוטציות שקטות".
למחקר החדש השלכות לכלל תחומי המחקר והטיפול האונקולוגי, ואחרי הוכחת ההיתכנות הזאת בכוונת החוקרים להקים סטארטאפ עם חממת "סאנרה", שיתמקד במוטציות השקטות ככלי רפואי לכל דבר ועניין.
עוד השתתפו במחקר: גיא גורן ועומרי עפרוני
למאמר ב npj genomic medicine
אלה שמתאהבים בבעיה הם אלה שממציאים לה את הפתרון